INTRODUCCIÓN.
 El sistema inmunológico está constituido por órganos, células y sus productos. Los órganos se han definido como primarios (aquellos donde se producen y maduran células del sistema inmune), en el adulto: médula ósea y timo. En el primero de ellos se da la hematopoiesis, es decir la maduración de todas las líneas celulares tanto linfoide, mieloide como eritroide. De allí también viaja temprano en la embriogénesis un progenitor linfoide inmaduro hacia el timo, donde completa su desarrollo hasta convertirse en linfocito T funcional, por tal motivo, el timo también es considerado un órgano linfoide primario (Lichtman, 1981). La línea linfoide produce en su maduración: linfocitos T, linfocitos B, linfocitos asesinos naturales (NK por sus siglas en inglés) y células dendríticas de linaje linfoide. La línea mieloide produce monocitos que maduran a macrófagos, neutrófilos, eosinófilos, basófilos, o también células dendríticas. Cada una de estas células tiene una función vital dentro del proceso de reconocimiento y respuesta a un agente extraño denominado antígeno.
El sistema inmunológico está constituido por órganos, células y sus productos. Los órganos se han definido como primarios (aquellos donde se producen y maduran células del sistema inmune), en el adulto: médula ósea y timo. En el primero de ellos se da la hematopoiesis, es decir la maduración de todas las líneas celulares tanto linfoide, mieloide como eritroide. De allí también viaja temprano en la embriogénesis un progenitor linfoide inmaduro hacia el timo, donde completa su desarrollo hasta convertirse en linfocito T funcional, por tal motivo, el timo también es considerado un órgano linfoide primario (Lichtman, 1981). La línea linfoide produce en su maduración: linfocitos T, linfocitos B, linfocitos asesinos naturales (NK por sus siglas en inglés) y células dendríticas de linaje linfoide. La línea mieloide produce monocitos que maduran a macrófagos, neutrófilos, eosinófilos, basófilos, o también células dendríticas. Cada una de estas células tiene una función vital dentro del proceso de reconocimiento y respuesta a un agente extraño denominado antígeno.
Dentro de los órganos linfoides secundarios se encuentran bazo, ganglios, placas de Peyer, amígdalas y adenoides (Erslev et al., 1990). En ellos se almacenan células del sistema inmune y generalmente allí ocurren respuestas inmunitarias posteriores al encuentro del antígeno, donde se involucran procesos de fagocitosis, presentación de antígeno, generación de anticuerpos y citoquinas. Un antígeno es cualquier molécula originada de un organismo vivo o no, que es considerada extraña por un organismo que posea sistema inmunológico. En el sentido estricto dicha molécula será un inmunógeno, si es capaz de desencadenar una respuesta en el organismo aceptor u hospedero. La aclaración debe hacerse porque todos los inmunógenos son antígenos, pero no todos los antígenos son inmunógenos. Esto quiere decir que a pesar de ser extraños, no son capaces de desencadenar una respuesta inmunológica. La capacidad de inducir tal respuesta inmunitaria, está asociada a factores como tamaño de la molécula, distancia filogenética con el organismo aceptor, complejidad de la molécula, vía de administración, dosis, etc. (Berzofsky y Berkower, 2003). Gracias al proceso de selección donde ocurre reconocimiento de antígenos propios (durante la maduración de células inmunes), las células maduras deben ser capaces de distinguir antígenos propios de extraños y activarse solo en respuesta a los últimos.
De tal manera, los antígenos pueden encontrarse en entidades complejas como virus, bacterias, parásitos, hongos o fracciones de ellos, hasta en moléculas como medicamentos o proteínas presentes en alimentos. Pueden penetrar por laceraciones en piel, por vía respiratoria, digestiva, venosa y mucosas. El sistema inmune tiene un régimen de alarma mediado por sustancias químicas y células (como neutrófilos) que reconocen de primera mano agentes agresores o sustancias extrañas, y son estos los que se encargan de avisar a los demás miembros del sistema inmune para que se recluten o migren al sitio de la infección para evitar crecimiento, proliferación y dispersión de dichos agentes agresores.
¿CÓMO SABE EL SISTEMA INMUNOLÓGICO QUE ALGO ES EXTRAÑO?
La capacidad de diferenciar antígenos propios de extraños, es el producto de estrictos procesos de selección, de células B y T; de tal manera que cuando son funcionales en la circulación, y encuentran un antígeno que no ha sido mostrado en su proceso de maduración, dichas células se pueden activar e inducir respuesta inmune.

imagen 1. se muestra la estructura general de los linfositos T y B
El proceso de maduración celular que ocurre en los órganos linfoides primarios, es costoso en términos de vida celular, pues gran porcentaje de las células que no logran selección positiva mueren por apoptosis (muerte celular programada). Durante esta maduración las células deben ser capaces de reconocer sus propias moléculas del complejo mayor de histocompatibilidad (CMH) presentando péptidos propios, pero no deben activarse (Palmer, 2003). Este proceso es posible porque, los antígenos propios pueden ser presentados como un -bufé- para que sean reconocidos por células que están en el proceso de maduración; se ha demostrado que esta capacidad de presentar antígenos de manera ectópica en el timo, está asociada con la expresión de un factor de transcripción denominado AIRE (Derbinski et al., 2001; Taniguchi y Anderson, 2011). De esa manera cuando una célula madura, es decir, su proceso ha sido exitoso y está cumpliendo su función en la periferia al encontrar células con un CMH extraño (Ej. células de un transplante) o un antígeno, dispara una serie de mecanismos que conducen a lo que se denomina activación y puede desencadenar procesos encaminados a limpiar ese agente sea fagocitándolo, marcándolo para ser fagocitado (opsonización), o destruyéndolo como es el caso de la muerte producida por linfocitos T citotóxicos o células NK.
El reconocimiento de un antígeno también puede ser mediado por los patrones moleculares asociados a patógenos (PAMPs), estas son moléculas que están presentes en virus, bacterias, hongos, parásitos y que no existen en el humano, por tal motivo son fácilmente reconocidas como extrañas (Akira et al., 2006). En el organismo aceptor u hos pedero existen receptores para tales moléculas, conocidos como receptores de reconocimiento de patrones o PRRs que se encuentran ubicados sobre la membrana celular, en plasma o intracelularmente; esta amplia distribución asegura que sea posible detectar antígenos que han penetrado al organismo por diversas vías (Akira et al., 2006). Dentro de los PRRs más conocidos se encuentran los receptores Toll-like (TLR), similares a aquellos descritos en la mosca de la fruta Drosophila melanogaster, donde también se ha demostrado su papel en inmunidad (Khush et al., 2001). Estos receptores pueden reconocer diferentes PAMPs y activar segundos mensajeros que desencadenan respuesta inmune (O Neill, 2006).
¿Qué es el Síndrome de Guillain-Barré?
El Síndrome de Guillain-Barré es un trastorno en el que el sistema inmunológico del cuerpo ataca a parte del sistema nervioso periférico. Los primeros síntomas de esta enfermedad incluyen distintos grados de debilidad o sensaciones de cosquilleo en las piernas. En muchos casos, la debilidad y las sensaciones anormales se propagan a los brazos y al torso. Estos síntomas pueden aumentar en intensidad hasta que los músculos no pueden utilizarse en absoluto y el paciente queda casi totalmente paralizado. En estos casos, el trastorno pone en peligro la vida - potencialmente interfiriendo con la respiración y, a veces, con la presión sanguínea y el ritmo cardíaco - y se le considera una emergencia médica. El paciente es colocado a menudo en un respirador para ayudarle a respirar y se le observa de cerca para detectar la aparición de problemas, tales como ritmo cardíaco anormal, infecciones, coágulos sanguíneos y alta o baja presión sanguínea. La mayoría de los pacientes se recuperan, incluyendo a los casos más severos del Síndrome de Guillain-Barré, aunque algunos continúan teniendo un cierto grado de debilidad.
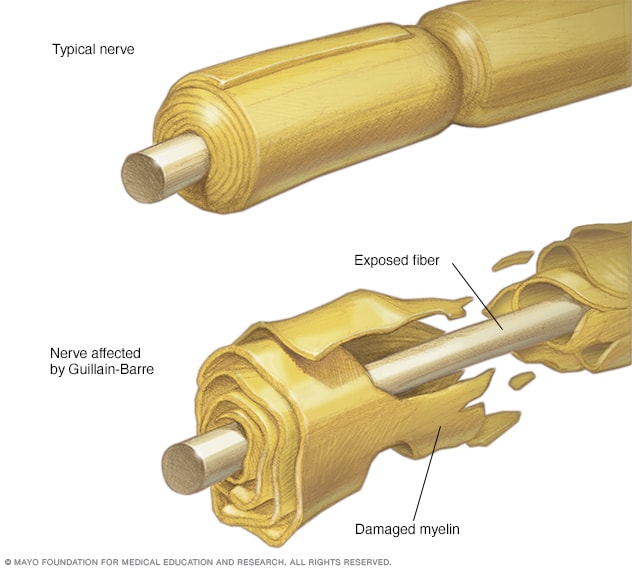
EL sistema inmunológico del cuerpo comienza a atacar al propio cuerpo, lo que se conoce como una enfermedad autoinmunológica. Comúnmente, las células del sistema inmunológico atacan sólo a material extraño y a organismos invasores. En el Síndrome de Guillain-Barré, no obstante, el sistema inmunológico comienza a destruir la cobertura de mielina que rodea a los axones de muchos nervios periféricos, o incluso a los propios axones (los axones son extensiones delgadas y largas de las células nerviosas que transmiten las señales nerviosas). El recubrimiento de mielina que rodea al axón acelera la transmisión de las señales nerviosas y permite la transmisión de señales a través de largas distancias.
En enfermedades en las que los recubrimientos de mielina de los nervios periféricos son lesionados o quedan afectados, los nervios no pueden transmitir señales con eficiencia. A ello se debe el que los músculos comiencen a perder su capacidad de responder a los mandatos del cerebro, mandatos que han de transportarse a través de la red nerviosa. El cerebro también recibe menos señales sensoriales del resto del cuerpo, resultando en una incapacidad de sentir las texturas, el calor, el dolor y otras sensaciones. Como alternativa, el cerebro puede recibir señales inapropiadas que resultan en cosquilleo de la piel o en sensaciones dolorosas. Debido a que las señales que van hacia y vienen desde los brazos y las piernas han de recorrer largas distancias, son las más vulnerables a interrupción. Por tanto, las debilidades musculares y las sensaciones de cosquilleo aparecen inicialmente en las manos y en los pies y progresan hacia arriba.
Cuando el Síndrome de Guillain-Barré va precedido de una infección viral, es posible que el virus haya cambiado la naturaleza de las células en el sistema nervioso por lo que el sistema inmunológico las trata como células extrañas. También es posible que el virus haga que el propio sistema inmunológico sea menos discriminador acerca de qué células reconoce como propias, permitiendo a algunas de las células inmunológicas, tales como ciertas clases de linfocitos, atacar la mielina. Los científicos están investigando éstas y otras posibilidades para determinar por qué el sistema inmunológico funciona mal o es perturbado en el Síndrome de Guillain-Barré y otras enfermedades inmunológicas. La causa y la trayectoria del Síndrome de Guillain-Barré es un área activa de investigación neurológica e incorpora los esfuerzos de colaboración de los científicos neurológicos, inmunológicos y virólogos.
¿Cómo se trata el Síndrome de Guillain-Barré?
No hay una cura conocida para el Síndrome de Guillain-Barré. Sin embargo, hay terapias que reducen la gravedad de la enfermedad y aceleran la recuperación en la mayoría de los pacientes. Hay también cierto número de formas de tratar las complicaciones de la enfermedad. Por lo general, la plasmaféresis y la terapia de inmunoglobulina de alta dosis son los remedios utilizados. Ambos son igualmente eficaces, pero la inmunoglobulina es más fácil de administrar. La plasmaféresis es un método mediante el cual se saca sangre entera del cuerpo y se procesa de forma que los glóbulos blancos y rojos se separen del plasma o la porción líquida de la sangre. Las células de la sangre se devuelven luego al paciente sin el plasma, el cual el cuerpo sustituye rápidamente. Los científicos no conocen todavía exactamente por qué funciona la plasmaféresis pero la técnica parece reducir la gravedad y duración del episodio de Guillain-Barré. Esto quizás se deba a que la porción del plasma de la sangre contiene elementos del sistema inmunológico y puede ser tóxico para la mielina.
En la terapia de inmunoglobulina de alta dosis, los médicos administran inyecciones intravenosas de proteína que, en cantidades pequeñas, el sistema inmunológico utiliza naturalmente para atacar a los organismos invasores. Los investigadores han descubierto que la administración de altas dosis de estas inmunoglobulinas, derivadas de un conjunto de miles de donantes normales, a pacientes de Guillain-Barré puede reducir el ataque inmunológico sobre el sistema nervioso.
Lo que se quiere lograr con este proyecto es determinar que genes están implicados en la inmunidad del cuerpo humano y por medio de estos cambiar el recubrimiento de ciertos genes en la celulas del sistema nervioso periférico de tal forma que se vuelva impenetrable ante un ataque del sistema inmune y así evitar que las células destruyan el tejido de mielina y no perjudiquen el sistema nervioso.
Comentarios
Publicar un comentario